
本文作者:热心肠研究院学术部数据科学家 高春辉博士
10月23日的《肠道产业》文章中,我们介绍了武田新药维多珠的最新真实世界研究数据,显示维多珠单抗(Vedolizumab,VDZ)在治疗中、重度活动性溃疡性结肠炎(UC)或克罗恩病(CD)中具有较好疗效。
延伸阅读:
UEGW:武田发布 IBD 真实世界研究结果,维多珠继续罕逢敌手!
今天,我们再来介绍一款已经在中国上市的新药——乌司奴单抗(Ustekinumab,UST),并了解一下 UST 的作用机制和创新点,以及与 VDZ 在机制存在什么差异。
UST 由美国强生公司研发。2019年6月5日,强生公司在华制药子公司西安杨森制药有限公司宣布:乌司奴单抗注射液在中国上市,商品名“喜达诺”。
虽然,UST 在中国上市的适应症目前不包括炎症性肠病(IBD),但是国际上的相关研究表明,UST 在治疗 UC 和 CD 这两种常见的 IBD 疾病时具有很好的疗效。
UST是全球首个全人源“双靶向”白介素抑制剂,同时作用于白介素12(IL-12)和白介素23(IL-23),通过特异性调节肠道固有免疫从而迅速缓解肠道免疫炎症状态,在适应性免疫中从上游阻断多种效应 T 细胞的分化,防止疾病不同表型转移,阻止IL17A 为主的炎症因子产生,达到 IBD 治疗的长期疗效。
IL-12和 IL-23都是异源二聚体细胞因子,有着共同的亚基 p40,位于信号转导的上游。IL-12和 IL-23的两个亚基分别与相应的受体结合后会激活 JAK2和 TYK2激酶,在下一步的转录因子激活层面,IL-12激活 STAT4,而 IL-23激活 STAT3和 STAT4转录因子,从而引发下游的一系列基因的表达,发挥其生物学功能。
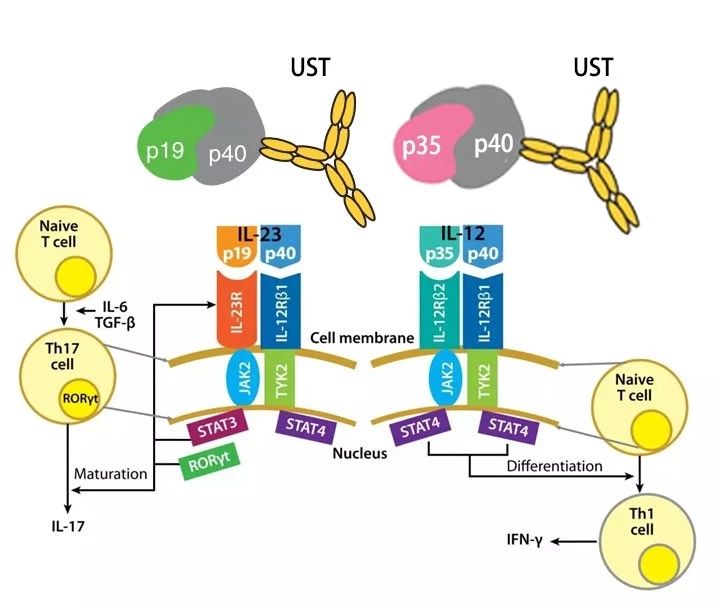
(图片改编自 Gastroenterol Hepatol 2019;15:255–265 和 Nature Biotechnology 2011;29:615–624)
UST 与 VDZ 的共同点都是生物药制剂。生物药的作用机制依赖于明确的细胞生物学过程机制的阐明,并在此基础上通过阻断特定生物学过程发挥作用。
与 UST 相比,VDZ 则是通过特异性拮抗 α4β7 整联蛋白,抑制整联蛋白与肠粘膜寻址细胞粘附分子-1(MAdCAM-1)的结合来发挥作用的。由此可见,UST 与 VDZ 的机制存在差异,这也是 UST 重要的创新点之一。
根据相关资料,我们整理了 UC 适应症的新型生物药临床实验进展。除了 VDZ 和 UST,目前还有多个“新药”(准确的说法应该是新适应症)已经做好了上市前的准备。
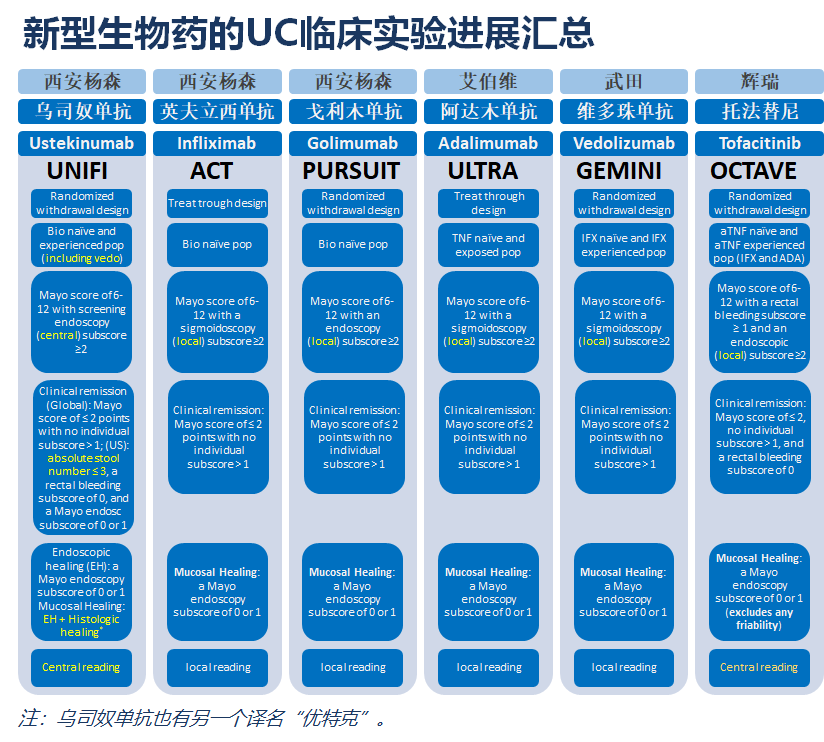
我们还欣喜的看到,UST 的临床实验中,采用了更严格的美国 MAYO 评分体系、中心读片(相比于其它研究 local reading 标准更统一)、终点检测组织学粘膜愈合情况。

我们看到,入组患者50%为既往使用过其它生物制剂的患者。在这样的条件下,UST 仍然取得了较好的临床实验结果,显得尤为可贵。
在《热心肠日报》中,收录了 UST CD适应症3期临床试验结果(NEJM,2016),以及 UC 适应症3期临床试验结果(NEJM,2019)。
New England Journal of Medicine——[IF:70.67]
① 乌司奴单抗是针对IL-12及IL-23的p40亚基的单克隆抗体;② 评估在中等及严重克罗恩病患者中,乌司奴单抗静脉诱导疗法,以及皮下维持疗法;③ 经过6周治疗后,相比于接受安慰剂的对照组,静脉注射乌司奴单抗的患者的响应率显著升高;④ 每8周或12周接受一次皮下注射维持剂量的乌司奴单抗的患者,在第44周时,相比于接受安慰剂的对照组,缓解率显著升高。
Ustekinumab as Induction and Maintenance Therapy for Crohn's Disease
2016-12-13, doi: 10.1056/NEJMoa1602773
【主编评语】一个新的对抗克罗恩病的抗体药物,针对IL-12及IL-23的p40亚基的单克隆抗体,推荐关注的人看一看。(@蓝灿辉 | 热心肠先生)
New England Journal of Medicine——[IF:70.67]
① 961名中重度溃疡性结肠炎患者分为3组,分别注射130mg、6mg/kg的乌司奴单抗或安慰剂;② 8周后,注射不同剂量乌司奴单抗用于诱导治疗的患者的临床缓解率均显著高于安慰剂组患者;③ 8周后,对诱导治疗产生应答的患者随机分为2组,每8周(部分为每12周)注射90mg的乌司奴单抗或安慰剂,用于维持治疗;④ 44周后,注射乌司奴单抗用于维持治疗的患者的临床缓解率显著高于安慰剂组患者;⑤乌司奴单抗组患者的不良事件发生率与安慰剂组相似。
Ustekinumab as Induction and Maintenance Therapy for Ulcerative Colitis
09-26, doi: 10.1056/NEJMoa1900750
【主编评语】New England Journal of Medicine上发表的一项3期临床试验结果,在近1000名中重度溃疡性结肠炎患者中,相比于安慰剂,静脉注射乌司奴单抗用于诱导治疗及维持治疗,均可显著提升患者的临床缓解率。(@沈志勋)
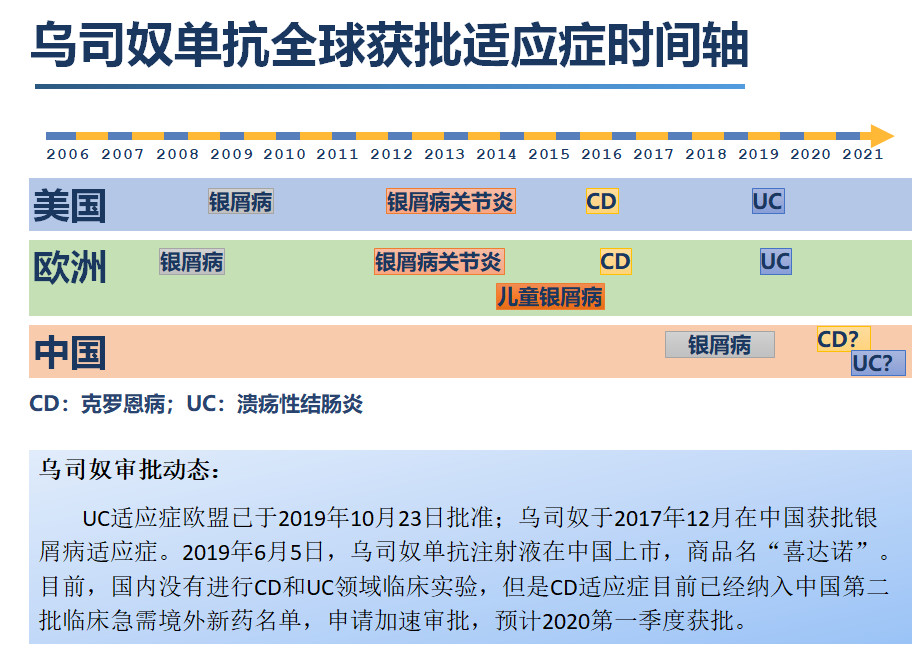
UST 在2009年和2013年分别被批准用于治疗银屑病和银屑病关节炎之后,于2016年被批准用于治疗 CD,2019年被批准用于治疗 UC。在全球拥有逾十年的临床使用数据,其有效性、安全性和依从性也已被大量真实世界研究验证。
在中国,UST 于2017年12月获批银屑病适应症,2019年上市。目前,国内还没有开展 CD 和 UC 的临床实验,但是 CD 适应症目前已经纳入中国第二批临床急需境外新药名单,有望在2020年获批。
虽然 UST 与 VDZ 的作用机制不同,但是它们都是通过降低人体免疫反应活性达到治疗效果的,即它们的本质都是免疫抑制剂。
免疫系统的过度反应是 IBD 直接的病因之一。除 IBD 以外,免疫系统失衡还会引起银屑病、强直性脊柱炎、类风湿性关节炎、系统性红斑狼疮和多发性硬化症等多种疾病。
所以,我们会看到图中 UST 的适应症包括银屑病、儿童银屑病等症状。
类似的,戈利木单抗的使用说明书中列入的适应症还包括类风湿性关节炎、强直性脊柱炎等病症;阿达木单抗的适应症还包括类风湿性关节炎、强制性脊柱炎、银屑病等病症。
由于相似的机理,靶向免疫系统生物药在治病的同时,由于免疫系统功能受到抑制,进行治疗的患者发生严重感染的风险增高。
报告的感染常见以下三种:
活动性结核病,包括潜伏性结核病的再激活;
侵袭性真菌感染,包括组织胞浆菌病、球孢子菌病、念珠菌病、曲霉病、芽生菌病和肺孢子菌病;
机会性感染,包括军团菌属、李斯特菌属等细菌感染、病毒感染或其他机会性感染。
除此之外,免疫抑制剂可能还会增加恶性肿瘤的风险。
不过,在临床治疗上,这些风险都是可控的。例如,在 UST 的使用说明书中明确提到:活动性肺结核患者严禁使用 UST 治疗,潜伏性结核杆菌应在接受UST 治疗前,先治疗结核杆菌感染等。因此,普通患者无需有不必要的担心。
对于需要生物药的患者而言,上述临床使用风险大多数时候应该不是主要矛盾,主要矛盾是药物的价格。
国际制药巨头 AbbVie(艾伯维)今年1月25日公布了2018年业绩,在公司全年2209.12亿元人民币的销售收入中,修美乐的销售额就占1344.6亿元,占比达61%,创下单种药品的年销售记录。
事实上,2012年开始,修美乐就登上了全球药物销售排行榜榜首,并且至今仍牢牢占据这一位置。不过,据《每日经济新闻》报道,2017年修美乐在国内医院的销售额仅为1800万元左右。在国内,修美乐的通用名就是阿达木单抗注射液。
据媒体报道,修美乐每一支的价格在7600元以上。按照使用说明书在维持期每两周注射一次计算,每年的花费约在20万元人民币。
根据国家统计局发布的《2018年居民收入和消费支出情况》报告,2018年全国居民人均可支配收入中位数24336元。其中,城镇居民人均可支配收入中位数36413元,农村居民人均可支配收入中位数13066元。
粗略估计下,仅使用阿达木一项,一名患者平均每年需要花费8年的积蓄来治病(以中位数可支配收入计),一般家庭可能无法承受这样的治疗费用。
UST 治疗 IBD 适应症的药物目前还未在中国通过审批和上市,其销售价格仍未可知,但估计也会与修美乐处于相当水平。
如何使阿达木、乌司奴这样的特效新药走进千家万户,造福广大人民,恐怕将成为医保部门、药品研发企业和商业保险公司等机构未来面临的挑战性课题。


