编者按:
2020 年 9 月 21~22 日,热心肠研究院携手 Swisse 斯维诗于线上举办了 GUT2020 系列活动之“微生态营养补充剂与肠道健康前沿论坛”,特邀 8 位嘉宾出镜发表了在线演讲,共同探讨如何通过营养改善微生态环境,助力肠道健康。

今天,我们特别整理并发布中国科学院北京生命科学研究院赵方庆老师的演讲视频及图文实录,以飨读者。
赵方庆
中国科学院北京生命科学研究院教授
中国科学院北京生命科学研究院“百人计划”研究员、中国科学院大学医学院岗位教授、优青基金获得者、首届北京市杰出青年基金获得者。
近年来,先后主持国家自然科学基金 7 项(青年、面上、培育、重点和优青等)、国家重点研发计划课题 3 项、国防科技创新特区项目、中国科学院“科技创新交叉与合作团队”项目和中科院院长特别奖基金等。
在 Gut、Genome Biology、Nature Communications、ISME 等刊物上发表通讯作者论文 40 余篇。


大家好,我叫赵方庆,来自中国科学院北京生命科学研究院。今天我给大家带来的演讲的题目是《母婴交互与新生儿肠道菌群的塑造》。

那么大家都非常关心我们下一代的健康成长,大家也好奇,新生儿的肠道微生物和成年人有什么差异?
他们之间最大的差异在于菌群结构的稳定性。和成年人相比,从刚刚出生的胎儿、新生儿,到一岁、两岁、三岁,他们的菌群的变化都是非常剧烈的。
大家可以看到,在刚刚出生的时候,他的菌群多样性相对来说比较低。那么随着年龄的增长,我们可以看到,他的微生物的多样性显著地提升。但是,他所受到的扰动的因素相对于成年人来说也更多、更为剧烈。所以他的菌群相对来说更加不稳定。
这就提示我们,今后要更为关注新生儿肠道的健康,因为这与他的生长发育、免疫等等关系非常密切。
那么首先,我们想去探索一下,新生儿和菌群是什么时候第一次发生接触的。这里面有正、反两方面的观点。
有的人认为,新生儿在出生之前并没有接触到微生物。只有当刚刚出生的时候,如果他是通过剖宫产,那么他首先接触到的是皮肤,或者体外的这种微生物。如果他是顺产,那么他首先接触到的,就是母亲的产道的微生物。
所以这个话题,其实也是困扰整个研究领域的一个核心问题。这个问题的根源在于,我们对菌群进行研究所采用的方法,要么是通过菌群的培养,要么是通过对菌群的测序,这里面总是难以避免外源微生物的这种干扰。

直到最近,2019 年发表在 Nature Medicine 上的一篇文章,它是不依赖于培养和这种测序的方法,直接通过电镜去观察胎儿的肠道之内到底有没有这种细菌样的这种结构。
它从妊娠中期流产的胎儿的肠道中,检测到这些颗粒状的、类似于细菌的这种结构。并且结合培养组学发现,它们确实是一类丰度虽然不高,但是有活性的,并且对新生儿肠道发育、免疫有影响的一类活的细菌。
所以我认为这个工作就很好的证明了,新生儿他接触到的微生物比我们的预期要更久、要更长。他在出生之前,就已经和微生物有了相互作用。

那么到底哪些因素影响了新生儿的菌群?首先第一个主要的因素就是分娩方式。就像刚才我所说到的,如果是顺产,那么新生儿的菌群更接近母亲的产道,而剖宫产更像外界环境。
所以最近就有研究来试图通过对新生儿的肠道或者皮肤菌群来进行干预,使得他通过剖宫产的时候,就可以恢复顺产所本应获得的菌群。所以这是非常有创意的一个想法。

第二个影响因素主要来源于对新生儿的喂养的方式的不同。大家知道,对新生儿,如果采用母乳喂养,那么大家往往认为,这个新生儿可能更为健康,因为他可以从母亲的乳汁当中来获得相应的、除了营养成分之外的免疫因子等等。
那么如果我们比较母乳喂养和配方奶喂养,我们可以发现新生儿的肠道菌群的差异也是非常大的。那么这个差异对新生儿的免疫力的影响,也会带来一个深远的一个作用。

第三个就是抗生素的使用。大家都可能会有喂养小孩的这样的一个经验,如果小孩儿在服用抗生素之后,你可能会发现,小孩的食欲可能有变化,那么粪便的形态等等也会有变化。
这是最近的一个工作。他们通过为期三年的跟踪研究,发现抗生素的使用对新生儿的肠道菌群产生非常明显的扰动作用。并且有意思的是,有的菌可以很快的在撤掉抗生素之后就得到恢复,而有的微生物受到的扰动就明显的较大。
所以这就提示我们在对小孩用药的时候,除了关注对他的病理的这种影响,我们也需要关注这种抗生素对新生儿菌群的这样的一个扰动作用。

第四个就是我们所生活的家居环境。家居的环境对于新生儿的呼吸道、肠道、体表菌群都会带来非常显著的这种影响。有人就发现,如果家里有饲养宠物的话,那么我们婴儿发生过敏和肥胖的风险就会显著的要低一些。
所以也应了我们经常说的一句老话“不干不净,吃了没病”。所以这就是说,过度清洁和干净的环境并不有利于新生儿他的肠道的健康,以及菌群的这种维持。

更为重要的一点,就是母婴之间的交互是如何影响新生儿菌群,包括新生儿肠道、呼吸系统的免疫、发育等等。这个图总结了母婴之间的交互的方式,以及它对新生儿的作用的效果。
从新生儿刚刚出生,包括在子宫之内,这个菌群就已经发生了这样的一个纵向的传递过程。出生之后,这种喂养的方式,包括家居环境,包括母亲的日常的看护,都会显著的改变或者塑造新生儿的健康以及他的菌群。
这里面,我们非常关注的一个话题就是,当母亲(包括孕妇)她生病之后,这样的一个病理的状态是如何影响新生儿的菌群的,包括新生儿的健康的。
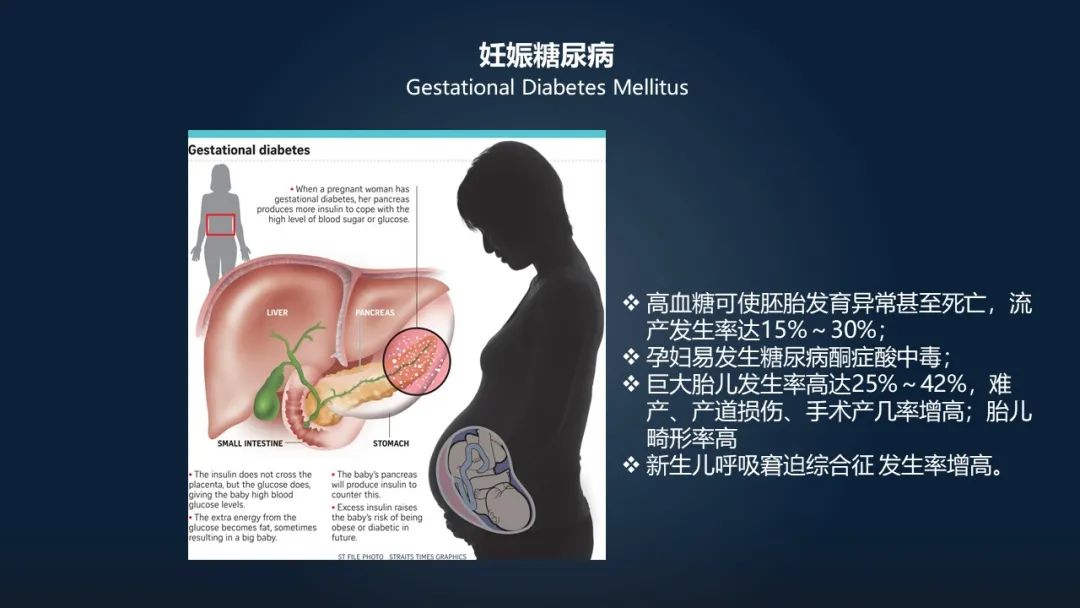
这里面,有一个高发的一个疾病是妊娠糖尿病。这种妊娠高血糖可能会促使胚胎发育异常,甚至死亡、流产的发生率也是非常高的。孕妇也容易发生这种糖尿病所导致的这种酮症酸的中毒现象。
而且,新生儿在出生的时候,体重也往往超标,导致难产、产道损伤,胎儿的畸形率相对也会有增加。新生儿在出生之后,所患这种呼吸窘迫综合症,它的概率也会显著的有提升。
最近我们和医院合作开展了这样一个工作:我们对孕妇,包括新生儿出生前后,孕产妇她的肠道、口腔和阴道的菌群,还包括新生儿的菌群进行了测定。
我们想关注的问题在于,新生儿的菌群到底是什么样子?他和母亲的菌群有多大的相似和相同之处?
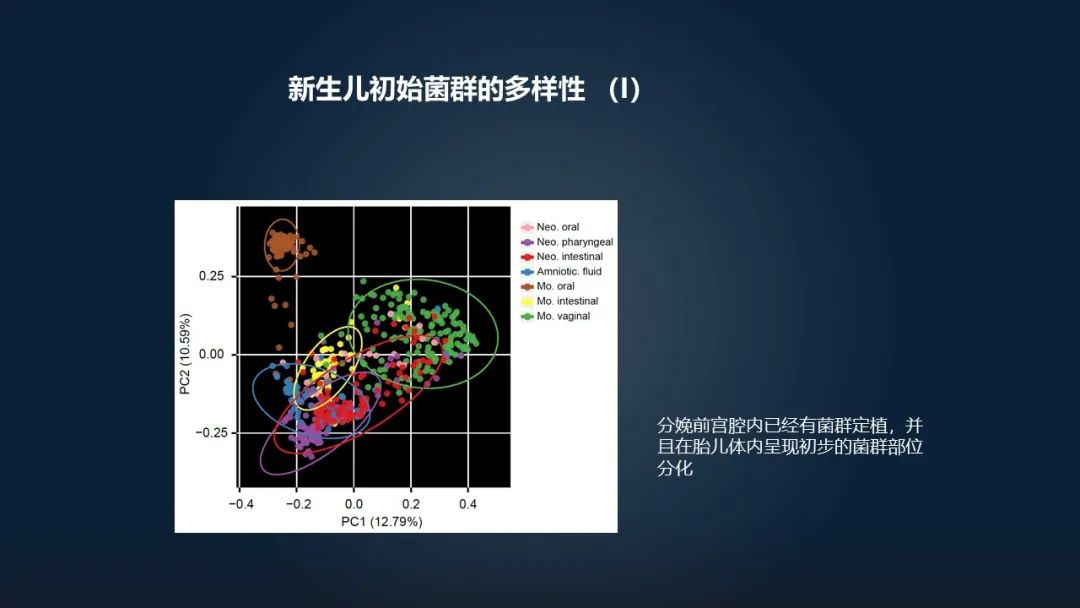
这里面我们就发现,早在出生之前,宫腔之内就已经有了大量的细菌的存在。在胎儿的不同的部位,他的菌群已经产生了初步的分化。我们可以非常清楚的看到,胎儿的口腔和他的肠道的微生物有着显著的差别。
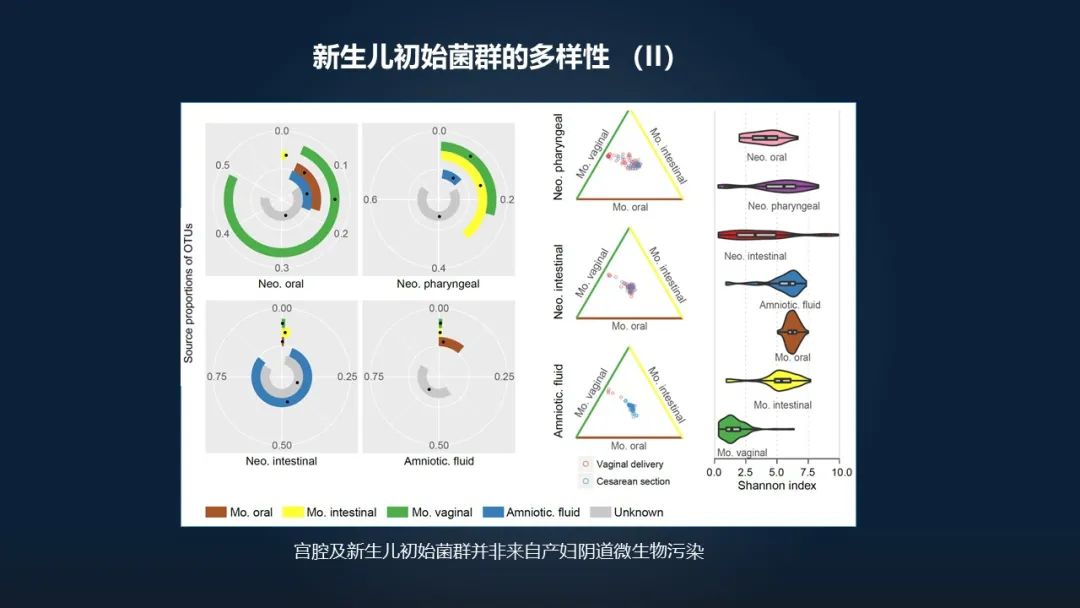
从这个比较的图上我们也可以看出来,新生儿的肠道微生物并不完全来自于产妇阴道微生物的污染。剖宫产的时候,他的菌群与产道并没有太大差异。对于顺产的这种胎儿,我们也可以看到,他的体表、口腔和肠道的微生物确实有一部分来自于这种母亲的阴道微生物。
如果我们计算它的物种的多样性,我们也可以看出来,尽管新生儿的微生物的数量并不多,但是它多样性和母亲的口腔、肠道在一个数量级上。这就说明,新生儿它的菌群的多样性是非常高的。
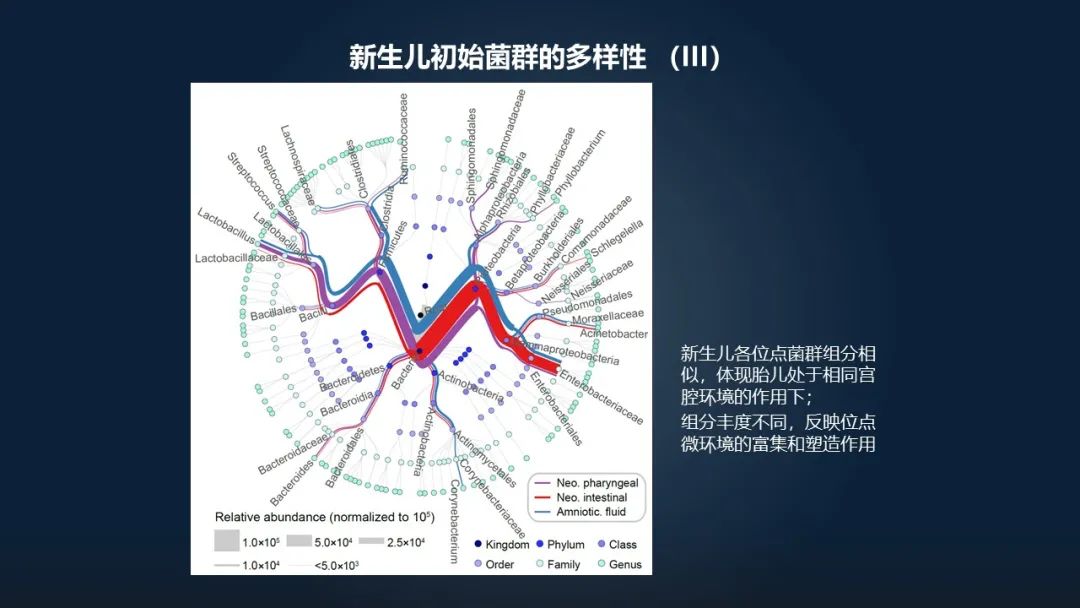
如果我们再看一下细节,看哪些类型的微生物占据了主导的地位,我们可以看到,新生儿的三个部位,口腔、肠道,包括羊水的微生物,它们之间大体上是类似的,菌群的组成上大体类似,但是相对丰度存在着显著的差异。
这就说明,尽管新生儿的肠道菌群的组分相似,但是由于不同的身体部位它所处的微环境并不相同,所以就导致这些微生物在各自的位点下所受到的选择压力存在显著的差异,所以他的菌群富集和塑造的这个过程并不相似。
我们除了关注健康的孕妇,以及她的新生儿的这种菌群,那我们想看,当孕妇得了病之后,特别是妊娠糖尿病之后,她的菌群到底有没有变化。
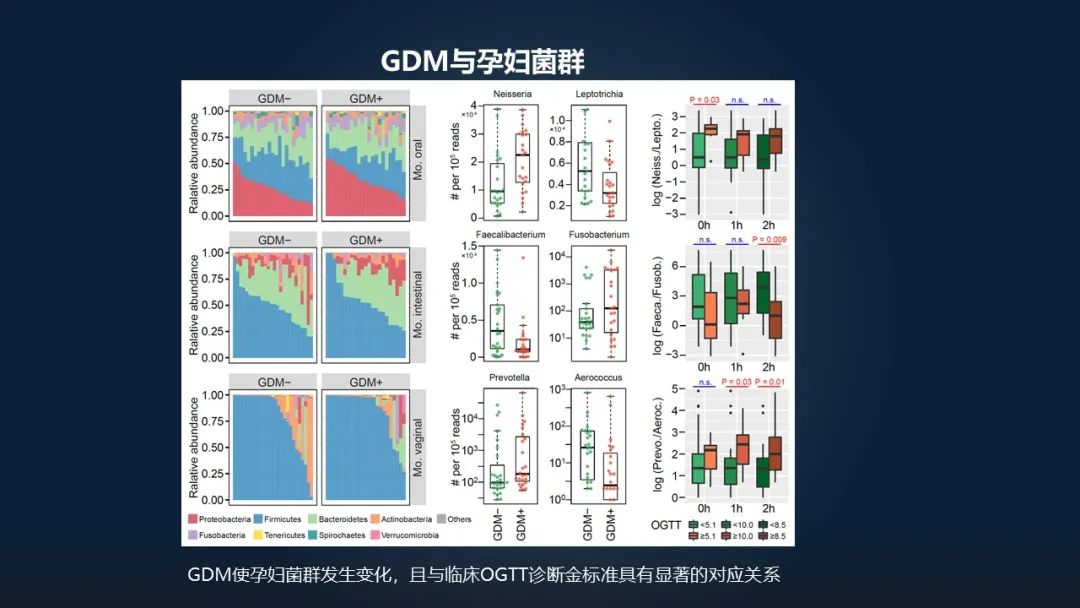
首先我们想去看 GDM(妊娠糖尿病)对孕妇菌群的影响。我们通过对孕妇口腔、肠道和阴道菌群的测定,我们也可以看到,健康和疾病之间都存在一定的差异,尤其是对于这种最上面这种口腔微生物的这种影响。
我们也可以看到左右两侧它的菌群在门的水平存在一个较大的差异,而对于像阴道和肠道的样本来说,它的差异尽管有,但是差异并不是那么显著。通过更精细的菌属的水平,我们也可以看到,某些特征性的菌属在两组之间存在显著的差异。
那么这个差异,到底与我们常规的这种临床诊断妊娠糖尿病的金标准——OGTT(口服葡萄糖耐量试验)这个值是不是存在对应关系?
我们结合临床的这种数据,我们可以非常清楚的看出来,这种微生物特征菌的这种变化的趋势和临床测定的这种糖耐实验它的诊断标准存在非常显著的相关性。
所以这里面就提出来一个潜在的、无创进行疾病诊断的一个新的一个标志物。我们是不是可以考虑采用对菌群、真菌来进行检测,通过它的含量的变化去评判这个孕妇是不是得了妊娠糖尿病?相对来说,这种诊断要更为简洁而快速。
我们既然可以看到 GDM 影响了母亲的菌群,那么对新生儿来说,它是不是也产生同样的这种影响?

我们通过针对羊水、口腔和新生儿的肠道微生物的测定,我们可以发现,它们之间也是存在差异的,并且这些差异与临床的诊断标准也有着显著的对应关系。
所以这里面就提出来一个很有意思的问题:疾病状态不仅影响母亲,也会影响新生儿,既然双方都有影响,那么这个影响的方向和趋势是不是一致?

这里面我们就结合各种各样的菌群和生物信息学的分析方法,通过重建两者的菌群的共现网络,我们可以看到,左右两侧分别是健康和疾病状态下这种菌群的改变。
我们可以看到特征菌它们之间有的是正相关,有的是负相关。那么这个相关性,在新生儿的肠道之内,我们可以看到它们非常显著的这种共现关系。那么也就意味着,一个差异的菌,如果出现在孕妇的体内,那么它也同等出现在她所出生的胎儿的、新生儿的这个肠道之内。
所以这就说明,疾病它不仅仅塑造了母亲的或者孕妇的她的肠道、口腔和阴道菌群,对于新生儿也会产生同样的这样的一个塑造作用。
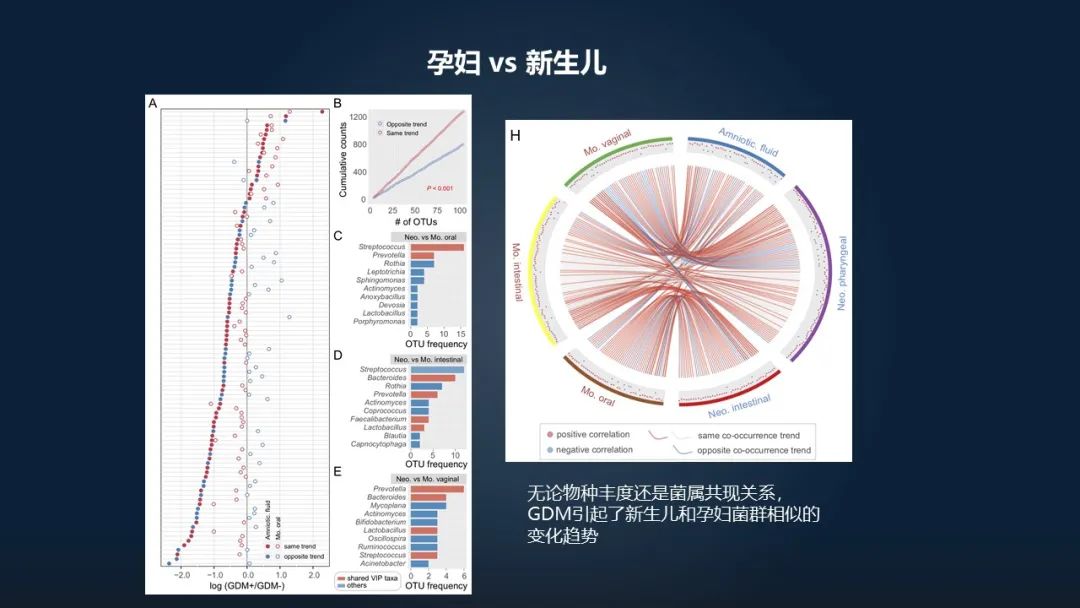
如果我们对它两者之间进行量化的话,我们可以看哪些菌更容易在两者之间——孕妇和新生儿之间发生变化,哪些菌不容易发生变化,以及这个变化是共同升高还是共同降低。
通过我们对它的物种丰度和共现关系,都可以看出来,它们所引起的新生儿和孕妇菌群都会产生同样的这种变化。比如右侧这个网络图上,我们也可以看出来,红色的代表的是同向的影响,蓝色的代表的是相反的影响。所以这种同向的塑造作用远远超过这种反向的塑造作用。
所以我们在关注孕妇的疾病的时候,其实我们也需要关心它对将来的新生儿所带来的这样的一个影响。
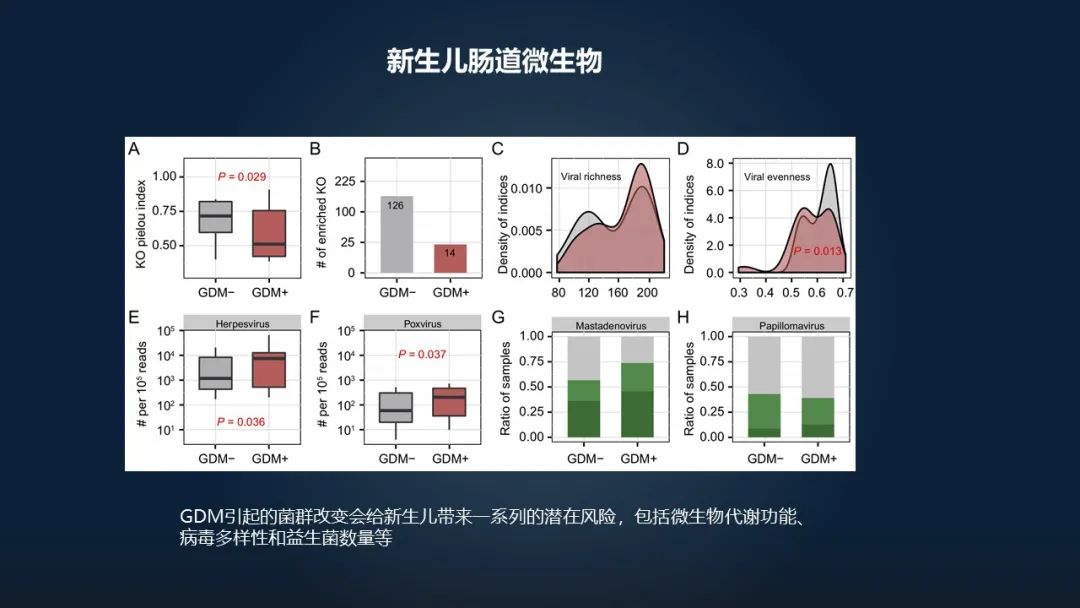
到底带来什么样的影响?
那我们通过对新生儿出生之后他的第一次胎便、他的菌群,包括他的菌群的功能来进行测定。我们可以看到,对于 GDM+,就是妊娠期糖尿病的孕妇所出生的胎儿,他的肠道之内的相应的毒力因子,包括病毒它的这种多样性显著的有提升,而益生菌的数量显著的有下降。
这就提示我们,新生儿可能存在着一系列的潜在的风险,包括后续的感染,或者是他对于代谢可能存在这样的一个缺陷。

总体来说,通过我们这样的一个研究,揭示了人体初始微生物的来源,通过亲子之间菌群的纵向传递过程,向我们展示了另外一种新的遗传形式——菌群遗传。
所以说我们的母亲不仅仅把她的基因传给我们,在她的 10 月怀胎期间,包括出生之后,通过对我们的抚养,她的微生物会源源不断的传递到新生儿的体内或体表。这里面,都对我们的新生儿的健康带来一个长期的一个影响。
通过这样的研究,我们也可以从全新的角度去思考孕期疾病,包括不良妊娠结局和产前菌群的联系。
那我们是不是可以考虑通过对菌群动态的监测,去管控这种孕期的健康,我们是不是可以通过对孕妇菌群的干预来可以帮助我们促进这种健康的生殖?
所以我们就通过这样的一个基础研究,可以帮助临床或者是将来的健康管理做出一些贡献。我也希望我们后续可以进一步的结合我们前期的工作基础,重点关注母婴之间菌群交互是如何影响和塑造新生儿菌群。
新生儿从出生到他的长大,这样的一个漫长的一个过程,0 到 3 岁是一个非常关键的一段时期。母亲所传递来的这些微生物是如何来演进的?
随着这种辅食的添加或者饮食的这种复杂化,外界引入的这些微生物是如何取代乃至演化为成年人所偏有的这样的一些肠道菌群的组成?
在整个过程当中,都充满了非常有意思的一些科学问题。我们也希望在将来的研究当中,能够得到一些新的发现,到时候再给大家汇报我们的工作。好,谢谢大家!



